1.教材P2
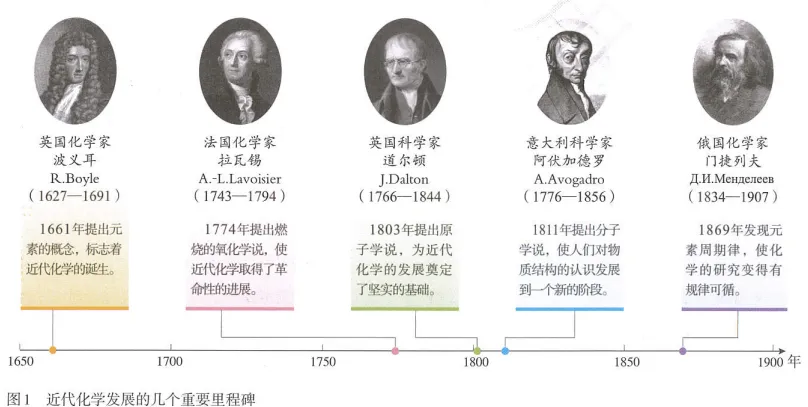
近代化学发展的几个重要里程碑:
1661年,英国化学家波义耳提出元素的概念,标志着近代化学的诞生。
1774年,法国化学家拉瓦锡提出燃烧的氧化学说,使近代化学取得了革命性的进展。
1803年,英国科学家道尔顿提出原子学说,为近代化学的发展奠定了坚实的基础。
1811年,意大利科学家阿伏加德罗提出分子学说,使人们对物质结构德认识发展到一个新的阶段。
1869年,俄国化学家门捷列夫发现元素周期律,使化学的研究变得有规律可循。
2.教材P3
21世纪以来,我国化学科学与技术发展的一些成就:
1943年,侯德榜发明联合制碱法,为我国德化学工业发展和技术创新作出了重要贡献。
1965年,我国科学家在世界上第一次用化学方法合成了具有生物活性的蛋白质——结晶牛胰岛素。
20世纪80年代,我国又在世界上首次用人工方法合成了一种具有与天然分子相同的化学结构和完整生物活性的核糖核酸,为人类揭开生命奥秘作出了贡献。
3.教材P8
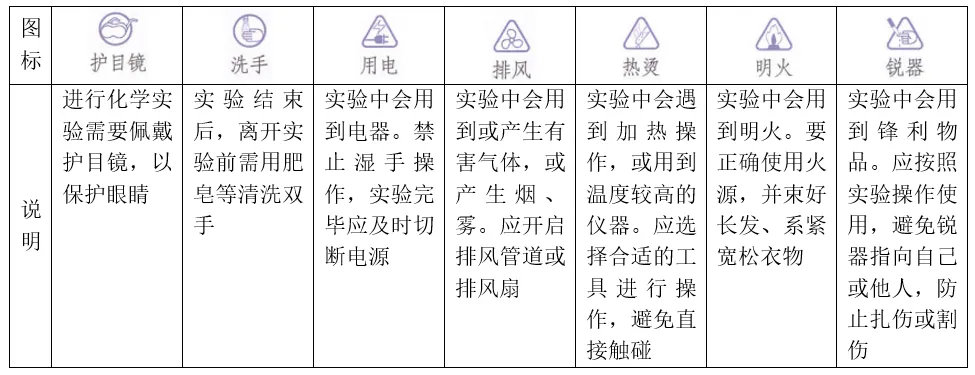
与实验有关的图标及说明
4.教材P9
当光束通过胶体时,看到的光柱是被胶体粒子散射的现象,并不是胶体粒子本身发光。
可见光的波长为400-700nm,胶体粒子的直径为1-100nm,小于可见光的波长,能使光波发生散射;溶液也发生光的散射,但由于溶液中粒子的直径小于1nm,散射及其微弱。所以,当光束通过胶体时可观察到丁达尔效应,而通过溶液时则看不到这种现象。

5.教材P11
要想制取某一种碱,通常可以采取两种方法:碱性氧化物与水反应;盐与另一种碱发生反应。
工业上制取NaOH一般不采用Na2O与H2O的反应(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用盐(如Na2CO3)与碱[如Ca(OH)2]反应的方法。
6.教材P12
【练习与应用】
T2.请从不同的角度对下列5种酸进行分类:盐酸(HCl)、硫酸(H2SO4)、硝酸(HNO3)、磷酸(H3PO4)和氢硫酸(H2S),并说出分类的依据。
酸的分类:(1)以是否含有氧元素为依据,可分为含氧酸和无氧酸(或称不含氧酸);(2)以每个分子中所含的氢原子个数为依据,可分为一元酸、二元酸、三元酸(其中二元酸和三元酸可以合称多元酸)。
T7.采用不同方法制取下列物质,并写出反应的化学方程式。
(1)以Fe、CuO、H2SO4三种物质为原料,用两种方法制取Cu。
(2)用三种方法制取MgCl2。
Cu的制备:(1)CuO+H2SO4=CuSO4+H2O Fe+CuSO4=FeSO4+Cu;
(2)Fe+H2SO4=FeSO4+H2↑ CuO+H2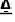 Cu+H2O。
Cu+H2O。
MgCl2的制备:(1)Mg+2HCl=MgCl2+H2↑;
(2)MgO+2HCl=MgCl2+H2O;
(3)Mg(OH)2+2HCl=MgCl2+2H2O。
T8.许多食品包装袋中常有一个小纸袋,内盛白色固体物质,标有“干燥剂”字样,其主要成分为生石灰。
(1)写出生石灰的化学式。生石灰属于哪一类别的物质?
(2)生石灰为什么可用作干燥剂(用化学方程式表示)?
(3)生石灰可以与哪些类别的物质发生化学反应?请列举两例,并写出反应的化学方程式。
(4)在你学过的物质中,还有哪些物质可用作干燥剂?
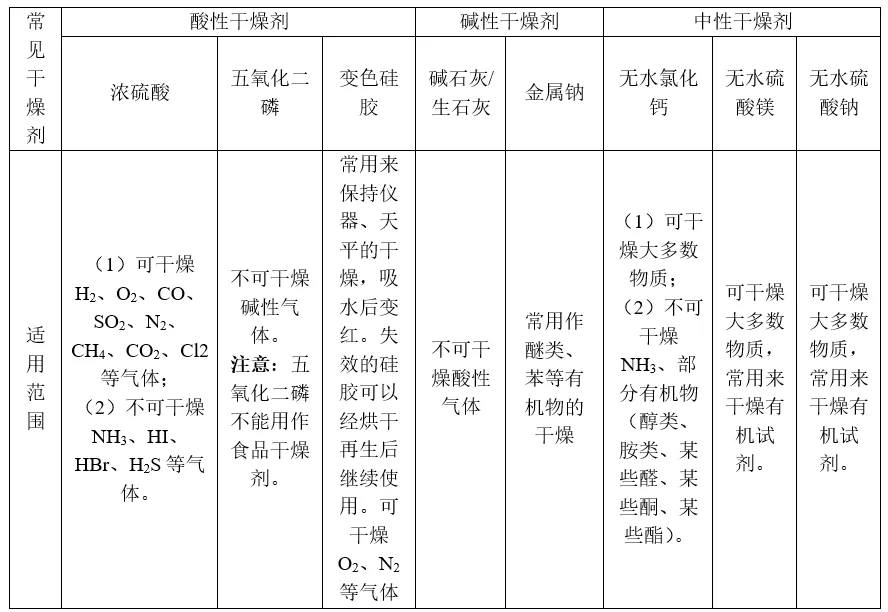
常见干燥剂及其适用范围:
7.教材P13
物质导电性实验中,蒸馏水也能导电,只是导电能力非常弱,用该实验装置不能测出。
8.教材P14
水合离子
当将NaCl固体加入水中时,在水分子的作用下,Na+和Cl-脱离NaCl固体的表面,进入水中,形成能够自由移动的水合钠离子和水合氯离子(如图1-11所示)。
9.教材P15
氢原子失去电子后,剩余1个质子构成的核,即氢离子。氢离子是“裸露”的质子,半径很小,易于水分子结合成水合氢离子,通常用H3O+表示。为了简便,也常把H3O+写作H+。
10.教材P16
阿伦尼乌斯电离模型

10.教材P23
氧化还原反应概念的发展

11.教材P24
生产生活中的氧化还原反应:金属的冶炼、电镀、燃料的燃烧、绿色植物的光合作用、易燃物的自燃、食物的腐败、钢铁的锈蚀等
12.教材P25【练习与应用】
T2.在高温时,水蒸气与灼热的炭发生氧化还原反应的化学方程式为:
H2O+C H2+CO
H2+CO
其中,H2O是______剂,C是______剂。
水煤气:(1)水煤气的成分为H2、CO;(2)水煤气制备原理:H2O+C H2+CO
H2+CO
T3.高温下铝粉与氧化铁的反应可以用来焊接铁轨。其原理是:该反应放出大量的热,置换出的铁呈熔融态。熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。该反应的化学方程式为_____________________,其中,还原剂是_______(填化学式,下同),被还原的物质是________。
铝热反应的应用:焊接钢轨。
T11.从氧化剂和还原剂的角度,分析下列三个反应中H2O2的作用。
(1)H2O2+H2S=2H2O+S↓
(2)H2O2+Cl2=2HCl+O2
(3)2H2O2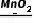 2H2O+O2↑
2H2O+O2↑
H2O2:既可作氧化剂,也可作还原剂,氧化性弱于Cl2。
T12.高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:
3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O
请分析上述反应中元素化合价的变化情况,指出氧化剂和还原剂。
高铁酸钠(Na2FeO4):新型绿色消毒剂,利用其强氧化性杀菌消毒,利用其还原产物Fe3+水解得到的Fe(OH)3胶体吸附难溶性杂质。
13.教材P29【复习与提高】
T2.维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有________(填“氧化性”或“还原性”)。
维生素C:还原剂,还原性,抗氧化性
补铁剂:补铁剂中铁元素以Fe2+形式存在,Fe3+不易被人体吸收,Fe2+易于吸收
T3.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:
S+2KNO3+3C=K2S+N2↑+3CO2↑
在该反应中,还原剂是______(填化学式,下同),被氧化的是______。
火药:火药成分为“一硫二硝(KNO3)三木炭”
T4.工业废水中含有的重铬酸铬离子(Cr2O42-)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:
6Fe2++Cr2O42-+14H+=6Fe3++2Cr3++7H2O
在该反应中,氧化剂是______(填离子符号,下同),被氧化的是______。
绿矾:FeSO4·7H2O
T5.在明代宋应星所著的《天工开物》中,有关于火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成团。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰’倭’云。”(注:炉甘石的主要成分是碳酸锌)。
(1)请完成上述火法炼锌反应的化学方程式:
ZnCO3+_____ _______+CO↑
_______+CO↑
(2)在该反应中,还原剂是______(填化学式,下同),被还原的是______。
火法炼锌:ZnCO3+2C Zn+3CO↑
Zn+3CO↑
炉甘石:ZnCO3
T10.在西汉刘安组织编撰的《淮南万毕术》中,有“曾青得铁则化为铜”的记载。这说明早在西汉时期,我国劳动人民就已经发现铁能从某些含铜(+2价)化合物的溶液中置换出铜,这个反应是现代湿法冶金的基础。下列关于该反应的说法中,不正确的是( )。
A.该反应说明铁的金属活动性比铜的强
B.该反应的离子方程式为:Fe+Cu2+=Fe2++Cu
C.该反应属于氧化还原反应,反应中铁被氧化
D.该反应说明金属单质都能与盐发生反应
湿法炼铜:“曾青得铁则为铜”,Fe+Cu2+=Fe2++Cu
14.教材P32
不能用手直接接触钠,而要用镊子夹取。

15.教材P33
不能近距离俯视坩埚。

16.教材P35
实验室将钠保存在石蜡油或煤油中。火灾现场存放有大量活泼金属时,不能用水而需要用干燥的沙土来灭火。
过氧化钠可在呼吸面具或潜水艇中作为氧气的来源
17.教材P36
Na2CO3的主要用途:纺织、制皂、造纸、造玻璃
NaHCO3的主要用途:制药、烘制糕点

18.教材P37
碳酸钠和碳酸氢钠的溶液均显碱性,可用作食用碱或工业用碱。
碳酸钠粉末遇水生成含有结晶水的碳酸钠晶体——水合碳酸钠(Na2CO3·xH2O)。碳酸钠晶体在干燥空气里逐渐失去结晶水变成碳酸钠粉末。
碳酸钠水合物有Na2CO3·H2O、Na2CO3·7H2O、Na2CO3·10H2O三种。
19.教材P37

20.教材P38
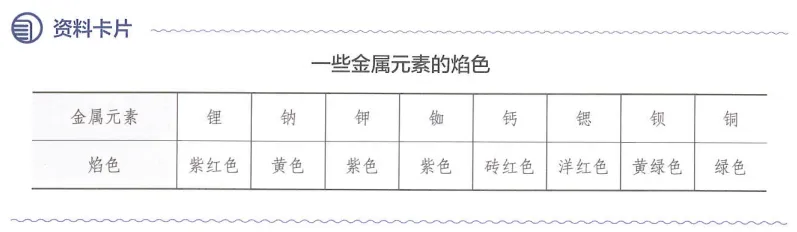
21.教材P42
氯气有毒,人吸入少量氯气会使鼻和喉头的黏膜受到刺激,引起咳嗽和胸部疼痛,吸入大量氯气会中毒致死。

22.教材P42
液氯与铁不反应,故液氯保存在钢瓶中。

23.教材P42
在25℃时,1体积的水可溶解约2体积的氯气,氯气的水溶液称为氯水。
24.教材P43
使用氯水对自来水消毒时,氯气会与水中的有机物发生反应,生成的有机氯化物可能对人体有害。
新型自来水消毒剂:二氧化氯(ClO2)、臭氧等。
25.教材P44
漂白液:有效成分:NaClO;主要成分:NaClO。
漂白粉:有效成分:Ca(ClO)2;主要成分:Ca(ClO)2、Ca(OH)2。
漂粉精:效成分:Ca(ClO)2;主要成分:Ca(ClO)2。
漂白液、漂白粉和漂粉精既可作漂白棉、麻、纸张的漂白剂,又可用作游泳池等场所的消毒剂。
26.教材P45
26.教材P47【练习与应用】
T1.下列生活中的物质与其有效成分的化学式、用途的对应关系中,不正确的是( )
选项 | A | B | C | D |
生活中的物质 | 食盐 | 小苏打 | 复方氢氧化铝片 | 漂白粉 |
有效成分的化学式 | NaCl | Na2CO3 | Al(OH)3 | Ca(ClO)2 |
用途 | 做调味品 | 做发酵粉 | 做抗酸药 | 做消毒剂 |
氢氧化铝的用途:抗酸药
T2.下列说法中,不正确的是( )。
A.燃烧一定伴有发光现象B.燃烧一定是氧化还原反应
C.燃烧一定要有氧气参加D.燃烧一定会放出热量
燃烧:伴有发光、放热的氧化还原反应都可以称为“燃烧”。
26.教材P50
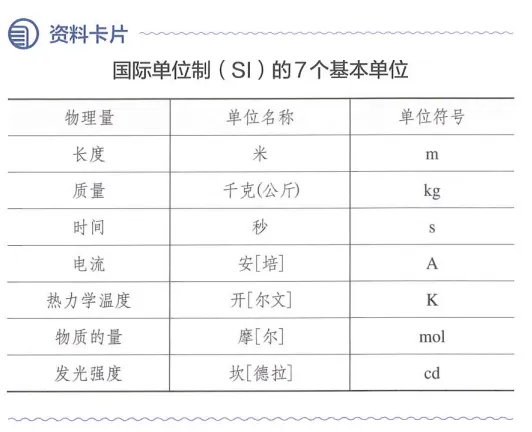
27.教材P53
气体摩尔体积的数值不是固定不变的,它取决于气体所处的温度和压强。例如,在0℃和101kPa(通常称为标准状况)的条件下,气体摩尔体积约为22.4L/mol;在25℃和101kPa的条件下,气体摩尔体积约为24.5L/mol。
28.教材P56【练习与应用】
T2.瓦斯中甲烷与氧气的质量比为1:4时极易发生爆炸,此时甲烷与氧气的体积比为( )
A.1:4B.1:2C.1:1D.2:1
瓦斯:主要成分为甲烷的易燃易爆炸气体。
29.教材P64
陨铁是从太空坠落于地球表面的含铁质较多的陨星。
30.教材P66

31.教材P67
FeO是一种黑色粉末,不稳定,在空气里受热,能迅速被氧化成Fe3O4。
Fe3O4是一种复杂的化合物,是具有磁性的黑色晶体,俗称磁性氧化铁。
Fe2O3是一种红棕色粉末,俗称铁红,常用作油漆、涂料、油墨和橡胶的红色颜料。
32.教材P73
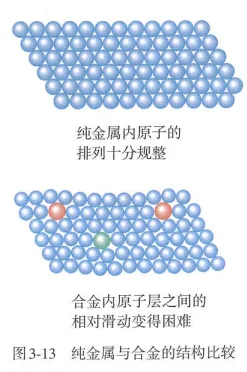
常见的一些合金的硬度比其成分金属大,是因为在纯金属内,所有原子的大小或形状都是相同的,原子的排列十分规整;加入或大或小的其他元素的原子后(如图3-13),改变了金属原子有规则的层状排列,使原子层之间的相对滑动变得困难,导致合金的硬度变大。
33.教材P74
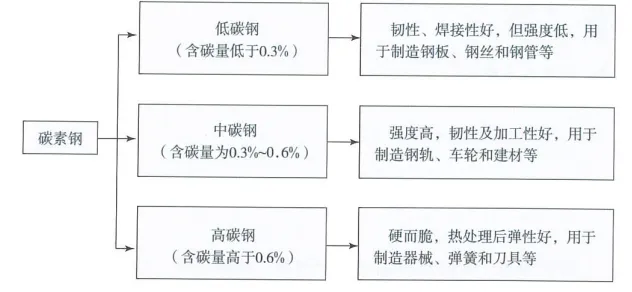
碳素钢的分类:
34.教材P74
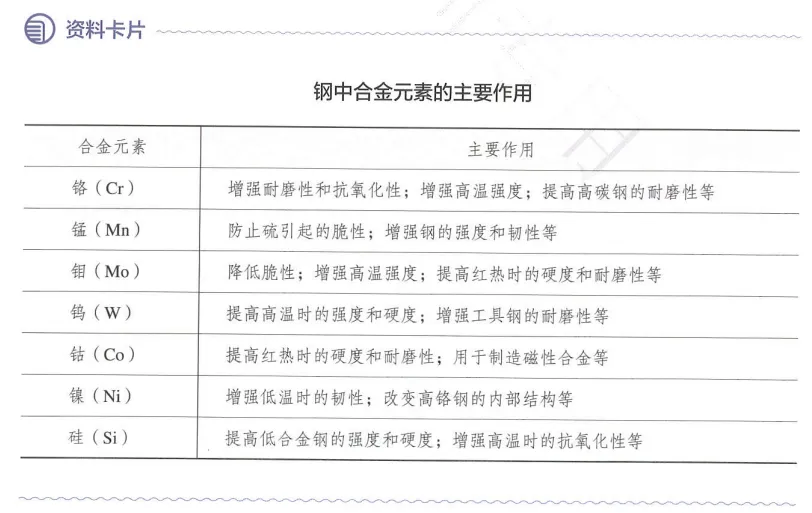
不锈钢的合金元素主要是铬(Cr)和镍(Ni)。
35.教材P76

36.教材P77
硬铝(一种铝合金)中含Cu4%、Mg0.5%、Mn0.5%、Si0.7%,它的密度小、强度高,具有较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料。

37.教材P77
新型合金:储氢合金(如Ti-Fe合金、La-Ni合金等)、钛合金、耐热合金、形状记忆合金等。


38.教材P77
稀土元素(“冶金工业的维生素”):元素周期表中原子序数从57-71(从镧至镥,称为镧系元素)的15种元素以及钪和钇,共17种元素。

39.教材P80【练习与应用】
T4.下列关于合金的说法中,正确的是()
A.合金的熔点一定比各成分金属的低
B.在我国使用最早的合金是钢
C.生铁的含碳量为0.03%-2%
D.稀土金属可以用于生产合金
合金的熔点不一定比各成分金属低,如汞合金。
40.教材P83【复习与提高】
T12.铁是人体必需的微量元素。请查阅资料回答以下问题:人体需要哪种价态的铁元素?哪类物质中的铁元素容易被人体吸收?哪些含铁物质适合做缺铁性贫血患者的补铁剂?
人体需要的铁为二价铁,可溶性的亚铁盐易被人体吸收。
常见补铁剂:硫酸亚铁、乳酸亚铁、琥珀酸亚铁等。
含铁较多食品:黑木耳、菠菜、蛋黄、动物内脏、铁强化酱油等。
41.教材P86
相对质量:指对12C原子质量的1/12(1.66×10-27kg)相比较所得的数值。
42.教材P88
原子结构模型的演变

43.教材P89
第Ⅷ族为副族,族序数后不标B。
44.教材P91
元素的相对原子质量,是按照该元素各种核素所占的一定百分比计算出来的平均值。
同位素的应用:考古时利用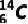 测定一些文物的年代;
测定一些文物的年代;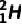 和
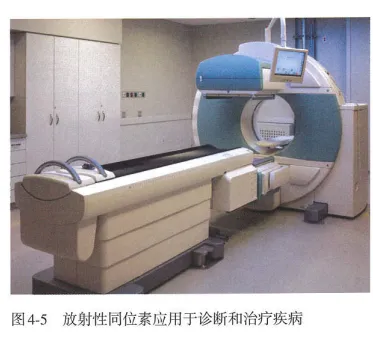
和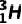 用于制造氢弹;利用放射性同位素释放的射线育种、给金属探伤、诊断和治疗疾病等。
用于制造氢弹;利用放射性同位素释放的射线育种、给金属探伤、诊断和治疗疾病等。
45.教材P92
元素周期表的发展

46.教材P93
金属的原子半径指固态金属单质里2个相邻原子核间距离的一半。
47.教材P95
液态钠可用作核反应堆的传热介质。
48.教材P101
稀有气体元素的原子半径测定与相邻非金属元素的测定依据不同,数据不具有可比性。
49.教材P105
周期表位置靠近的元素性质相近,在一定区域内寻找元素、发现物质的新用途被视为一种相当有效的方法。例:
在周期表中金属与非金属的分解处可以找到半导体材料,如硅、锗、镓等;对氟、氯、硫、磷、砷等元素附近区域进行研究,有助于制造出新品种的农药;在过渡元素中寻找制造催化剂和耐高温、耐腐蚀合金的元素。

50.教材P110
分子间作用力

51.教材P116
实验室突发事件的应对措施和常见废弃物的处理方法

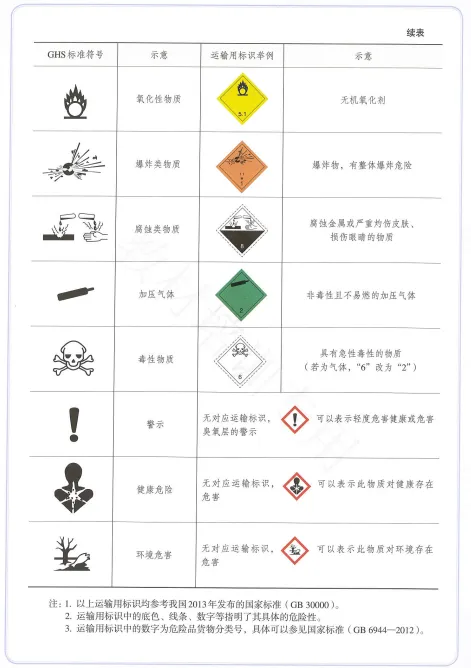
52.教材P117
一些化学品安全使用标识

长按上方二维码,点个关注再走吧!